|
علوم تجربی
اموزشی تفریحی
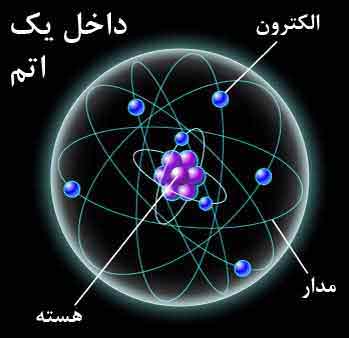
جمعه 28 بهمن 1390برچسب:, :: 1:30 :: نويسنده : نژادعلی نیلز بور فیزیکدان دانمارکی در زمینه چگونگی طیف نشری خطی اتم عناصر با پذیرفتن مدل اتمی رادرفورد چنین پیشنهاد داد که الکترونها در اطراف هسته اتم در سطوح انرژی مشخصی قرار دارند و در این سطوح به دور هسته اتم در حال چرخش هستند. انرژی الکترونهایی که در سطوح انرژی پایین تر به هسته نزدیکتر هستند، نسبت به الکترونهایی که از هسته دورند، انرژی کمتری دارند. پس برای انتقال الکترون از سطح انرژی پایین به سطح انرژی بالا، باید انرژی معادل اختلاف انرژی بین آن دو سطح را به آن الکترون بدهیم. پس انرژی الکترونها در یک اتم کوانتیده (گسسته) است.
مدل اتمی بور نشان داد که طیف نشر خطی که از اتم عناصر گسیل میشود، بر اثر انتقال الکترونها از سطوح انرژی بالا به سطوح انرژی پایین است، که در این انتقال انرژی الکترون کاهش مییابد و به صورت نور و گرما آزاد میشود. اگر نور آزاد شده را از منشور عبور دهیم طیف نشری آن مشخص میشود. بور مدل اتمی خود را بر اساس آزمایشهایی که با اتمهای هیدروژن و هلیم انجام شده بود مطرح میساخت به همین دلیل مدل اتمی او (که به مدل منظومه شمسی معروف است) برای اتمهای سنگینی مانند اورانیوم، آهن و ... صدق نمیکرد. به همین دلیل مدل اتمی کوانتمی (یا ابر الکترونی) با همکاری بسیاری از دانشمندان مانند هایزنبرگ، پلانک و شرودینگر مطرح شد. البته اینشتین با ارائه فرمولهای خود نیز توانست به این مدل اتمی کمک کند .
منبع : ويكيپديا
نظرات شما عزیزان:
موضوعات آخرین مطالب پیوندهای روزانه |
||
|
|